Vi rút Tembusu lần đầu tiên được phát hiện ở Việt Nam vào năm 2019, nó có khả năng lây lan nhanh qua đường tiếp xúc trực tiếp, gián tiếp hoặc qua côn trùng truyền bệnh. Sự lây lan này đã tạo ra một thách thức lớn trong công tác kiểm soát và phòng ngừa dịch bệnh ở đàn gia cầm. Trong bài viết này, cùng
Fivevet tìm hiểu phương pháp thiết lập phản ứng trung hòa định lượng kháng thể kháng vi rút Tembusu trên vịt, nhằm nâng cao hiệu quả trong việc kiểm soát và ngăn chặn dịch bệnh.

I. Tầm quan trọng của việc tầm soát kháng thể kháng vi rút Tembusu
Khi nhiễm vi rút Tembusu, triệu chứng lâm sàng thường thấy ở vịt đẻ bao gồm giảm sản lượng trứng đột ngột từ 80-90% xuống dưới 10% trong vòng 1-2 tuần, tiêu chảy phân xanh, suy nhược và các biểu hiện thần kinh như đi lại bất thường, khó khăn hoặc bị liệt, với tỷ lệ chết dao động từ 5-15% tùy vào điều kiện chăm sóc. Ở vịt con và vịt thịt, các triệu chứng bao gồm giảm ăn đột ngột, sinh trưởng chậm, tiêu chảy phân trắng, loãng, chảy nước mũi và các biểu hiện thần kinh như mất thăng bằng, vịt nằm lật ngửa, chân tê liệt. Tỷ lệ mắc bệnh có thể lên đến 90%, trong khi tỷ lệ chết dao động từ 5-30% tùy theo điều kiện nuôi dưỡng.
Bệnh tích do vi rút Tembusu gây ra thường xuất hiện ở nhiều cơ quan: Gan sưng to, nhạt màu; Dạ dày cơ bong tróc, xuất huyết ở dạ dày tuyến; Niêm mạc ruột có xuất huyết lan tràn; Phù não, màng não có các điểm xuất huyết lan tràn; Tim xuất huyết, có xuất hiện các vệt vằn.
Hiện nay một số loại vắc xin được sử dụng để phòng bệnh Tembusu như vắc xin sống giảm độc lực hoặc vắc xin bất hoạt. Trên thị trường Việt Nam, hiện nay vắc xin của tập đoàn Sinder Trung Quốc sản xuất và được nhập về Việt Nam theo đường chính ngạch do Công ty Invet nhập khẩu, còn lại hầu hết vắc xin trôi nổi, chưa được cấp phép lưu hành, nhập về Việt Nam qua các con đường tiểu ngạch, không được kiểm nghiệm đảm bảo được tiêu chuẩn chất lượng và cũng không đáp ứng đúng yêu cầu trong bảo quản và vận chuyển vắc xin của nhà sản xuất khuyến cáo. Vì vậy, khi sử dụng những loại vắc xin này không đảm bảo tính an toàn và hiệu quả phòng bệnh, nhiều đàn chủng ngừa vắc xin vẫn xảy ra dịch bệnh. Đây còn là nguy cơ gây ra sự tái tổ hợp các chủng vi rút gây nguy hại cho đàn vật nuôi.
Đáp ứng miễn dịch của vi rút Tembusu bao gồm cả gồm miễn dịch dịch thể và miễn dịch tế bào. Tuy nhiên, vi rút có khả năng lẩn tránh miễn dịch bẩm sinh bằng cách ức chế con đường IFN-α/β và giảm biểu hiện của MHC lớp I, giúp vi rút tránh bị tiêu diệt bởi tế bào T gây độc (CTLs). Đáp ứng miễn dịch dịch thể đóng vai trò quan trọng trong việc bảo vệ vật chủ chống lại vi rút Tembusu, bao gồm kháng thể trung hòa (Neutralizing Antibodies - NAbs) chống lại protein vỏ (E) của vi rút, giúp ngăn chặn vi rút xâm nhập và nhân lên trong tế bào và kháng thể dịch thể IgM và IgG. Để đánh giá miễn dịch dịch thể chống lại vi rút Tembusu, trên thế giới đã phát triển các phương pháp như phương pháp ngăn trở ngưng kết hồng cầu (HI), phương pháp ELISA và xét nghiệm trung hòa (VNT). Trên thực tế, phương pháp trung hòa được cho là "tiêu chuẩn vàng" để đánh giá mức độ bảo hộ của vắc xin với các chủng đang lưu hành tại thực địa.
II. Ứng dụng của phương pháp trung hòa vi rút Tembusu trên tế bào
2.1. Với những trại chưa tiêm phòng vắc xin:
Kết quả kháng thể Dương tính ở vịt chưa tiêm phòng vắc xin, đồng thời vịt có các đặc điểm dịch tễ học, triệu chứng lâm sàng của bệnh Tembusu được xác định là vịt đang bị mắc bệnh Tembusu. Vì vậy, việc định kỳ kiểm tra kháng thể Tembusu có ý nghĩa dịch tễ học để biết được sự lưu hành của vi rút.
2.2. Với những trại đã tiêm phòng vắc xin:
Phương pháp VNT được sử dụng như là công cụ giám sát và đánh giá hiệu quả tiêm phòng vắc xin, định lượng kháng thể có đạt mức bảo hộ (chỉ số GMT, PD50, tỉ lệ bảo hộ,…), độ đồng đều của kháng thể trong toàn đàn (chỉ số CV và SE).
Phương pháp VNT cũng được sử dụng đánh giá mức độ bảo hộ với chủng vi rút lưu hành tại thực địa, trong trường hợp tiêm phòng vắc xin Tembusu nhưng dịch Tembusu vẫn nổ ra gây thiệt hại tại các trại. Điều này có thể do biến chủng vi rút Tembusu. Tại Fivevet chúng tôi tiến hành phân lập, thu thập chủng Tembusu trên thực địa. Những chủng vi rút phân lập này được sử dụng để đánh giá mức độ bảo hộ khi sử dụng vắc xin Tembusu với chủng lưu hành tại thực địa. Từ đó, đánh giá tỉ lệ bảo hộ thực tế của vắc xin và có chiến lược lựa chọn vắc xin phù hợp.
III. Thiết lập phản ứng trung hòa vi rút Tembusu trên tế bào
3.1. Nguyên lý
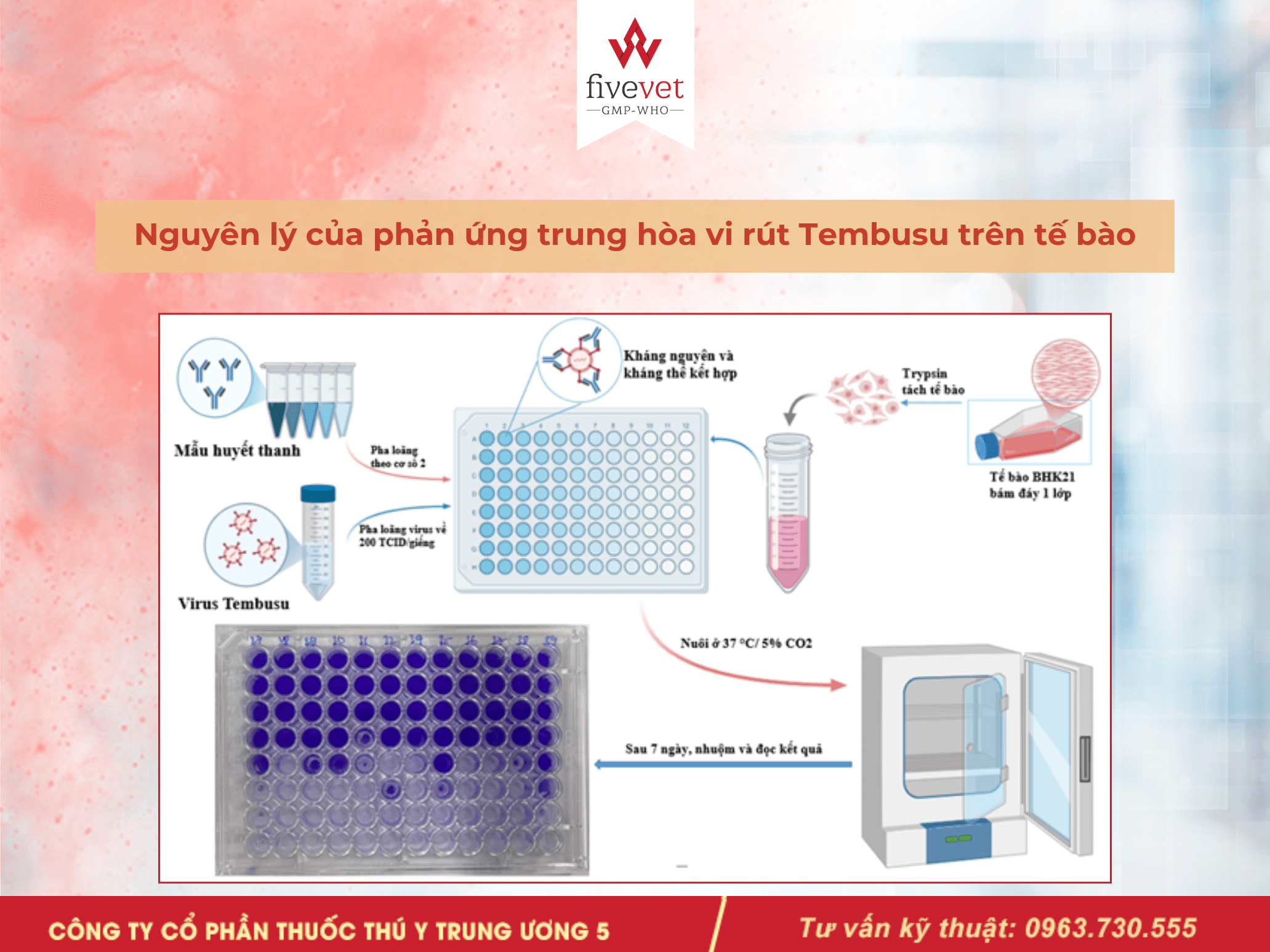
3.2. Quy trình thực hiện
3.2.1. Chuẩn bị mẫu xét nghiệm:
Mẫu huyết thanh để phát hiện kháng thể cần được lấy từ máu đã qua quy trình vô trùng, với lượng tối thiểu là 1 ml. Sau khi lấy mẫu, máu được để đông và sau đó tách huyết thanh. Mẫu huyết thanh cần được bảo quản trong điều kiện nhiệt độ từ 2°C đến 8°C. Mẫu máu sau khi đông sẽ được ly tâm lạnh ở tốc độ 4000 vòng/phút trong 10 phút để thu được huyết thanh. Đối với huyết thanh vịt, sau khi xử lý qua nhiệt ở 56°C trong 30 phút, tiếp tục xử lý kháng sinh trong 60 phút.
3.2.2. Chuẩn bị huyễn dịch tế bào:
Tế bào BHK21 khi đã bám thành lớp trên đáy sẽ được xử lý bằng trypsin để tách thành huyễn dịch, tạo thành dạng huyền phù với mật độ tế bào đạt 3x10^5 tế bào/ml.
3.2.3. Tiến hành phản ứng trung hòa vi rút:
Huyết thanh được pha loãng với tỷ lệ 1/2 đến 1/256 trong môi trường DMEM. Sau đó, 50 µl huyết thanh đã pha loãng sẽ được ủ cùng với 50 µl vi rút Tembusu, có mật độ 200 TCID50. Quá trình ủ sẽ diễn ra trong 1 giờ tại nhiệt độ 37°C. Sau đó, thêm 100 µl huyễn dịch tế bào BHK21 có mật độ 3x10^5 tế bào/ml vào hỗn hợp. Mẫu sẽ được nuôi cấy trong điều kiện 37°C, 5% CO2 trong 7 ngày. Cuối cùng, tế bào được cố định bằng formalin và nhuộm tím Violet để tiến hành đọc kết quả.
3.3. Đánh giá và phân tích kết quả:
Kết quả dương tính sẽ thể hiện bằng màu tím sau khi nhuộm, trong khi kết quả âm tính sẽ là những giếng không có màu (trống). Hiệu giá kháng thể được xác định là nồng độ pha loãng cuối cùng mà tại đó mẫu huyết thanh cho kết quả dương tính, tức là bào bắt màu thuốc nhuộm. Hiệu giá kháng thể được tính theo công thức 2n, trong đó n là hệ số pha loãng của huyết thanh.
Việc phân tích kết quả dựa trên các chỉ số như GMT, chỉ số bảo vệ PD50, tỷ lệ bảo vệ, chỉ số độ biến thiên CV% và chỉ số độ lệch chuẩn kháng thể SE.
Hình ảnh minh họa sẽ thể hiện quá trình chuẩn độ vi rút Tembusu và phản ứng trung hòa sau khi nhuộm.

 IV. Xác nhận giá trị sử dụng của phản ứng VNT trong việc xác định kháng thể kháng vi rút Tembusu
IV. Xác nhận giá trị sử dụng của phản ứng VNT trong việc xác định kháng thể kháng vi rút TembusuCác thông số để xác nhận giá trị sử dụng của phương pháp này bao gồm: độ chính xác (bao gồm độ đúng và độ chụm), độ nhạy và độ đặc hiệu.
Mẫu chuẩn dùng để xác nhận giá trị sử dụng của phương pháp trung hòa:
- Mẫu dương tính: 20 mẫu huyết thanh vịt có kháng thể kháng vi rút Tembusu, xác định qua phương pháp ELISA.
- Mẫu âm tính: 20 mẫu huyết thanh vịt từ những con không tiêm vắc xin Tembusu, xác định không có kháng thể kháng vi rút Tembusu qua phương pháp ELISA.
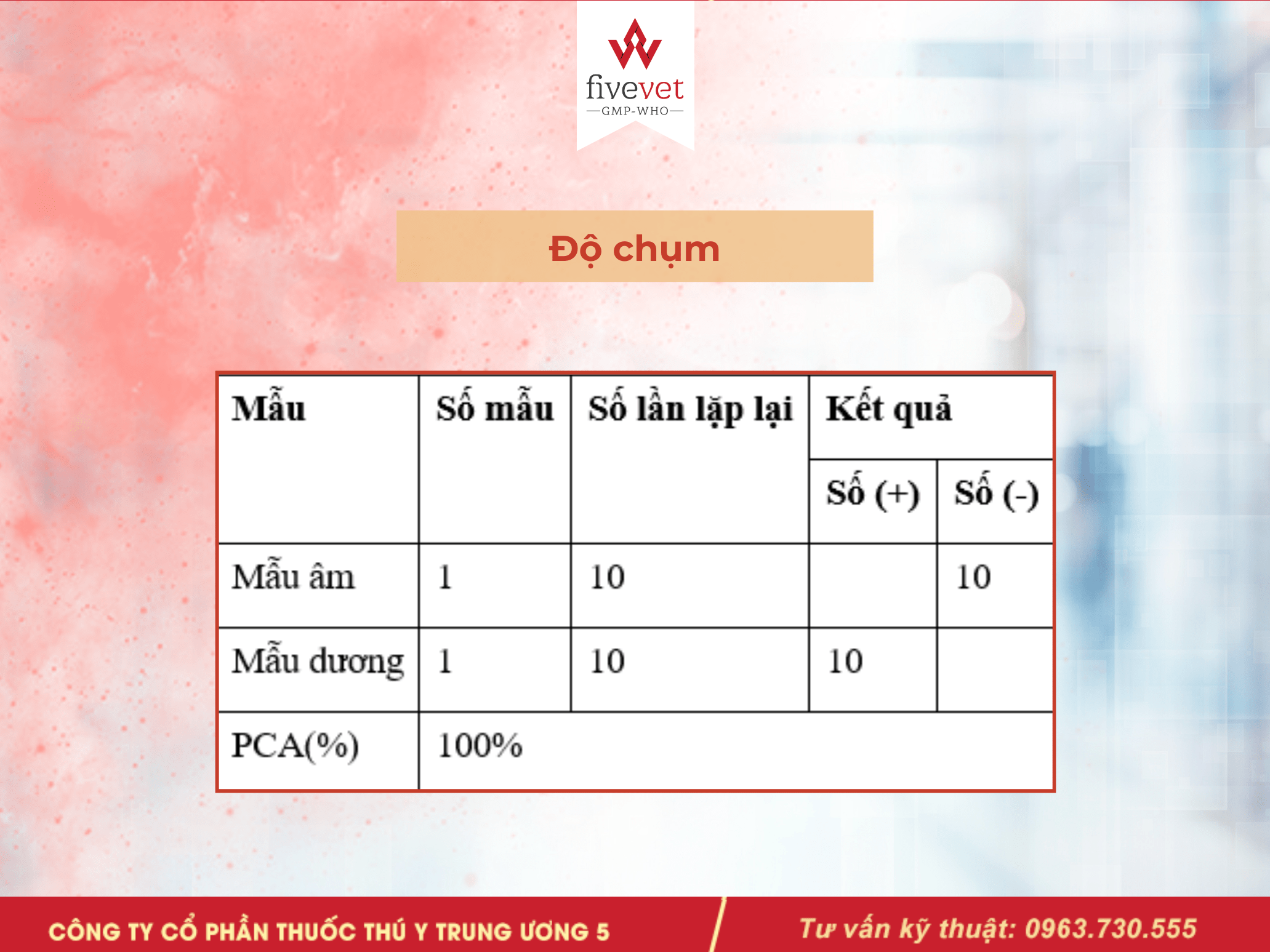
4.1. Độ chụm:
- Mẫu sử dụng: 1 mẫu huyết thanh dương tính và 1 mẫu huyết thanh âm tính.
- Thực hiện lặp lại thí nghiệm 10 lần.
- Để xác định độ chụm, sử dụng công thức PCA (Precision Categorical Agreement):
PCA(%) = X/N x100
Trong đó:
+ X là số lần kết quả không sai lệch ±1 log2.
+ N là tổng số lần thử nghiệm.
- Tiêu chuẩn: PCA(%) phải đạt ≥ 95%.
4.2. Độ đúng:
- Mẫu sử dụng: 20 mẫu huyết thanh dương tính và 20 mẫu huyết thanh âm tính.
- Để xác định độ đúng, sử dụng công thức CA (Categorical Agreement):
CA(%) = Y/N x100
Trong đó:
+ Y là số kết quả không sai lệch ±1 log2.
+ N là tổng số lần thử nghiệm.
Tiêu chuẩn: CA(%) ≥ 90%.

4.3. Độ nhạy và độ đặc hiệu:
- Mẫu sử dụng: 20 mẫu huyết thanh dương tính và 20 mẫu huyết thanh âm tính.
- Để xác định độ nhạy SE (Sensitivity) và độ đặc hiệu SP (Specificity):
SE(%) = a/(a+c) x100
SP(%) = d/(d+b)x100
- Tiêu chuẩn: SE(%) ≥ 90%, SP(%) ≥ 90%

Nếu nghi ngờ đàn vịt mắc bệnh, hãy liên hệ ngay Trung tâm Chẩn đoán Xét nghiệm và Kiểm nghiệm Thú y Trung Ương 5 (
FiveLab) theo số hotline 0822 120 555 để được tư vấn hỗ trợ kịp thời.
Xem thêm: