Tình hình dịch tễ PRRS tại Việt Nam diễn biến phức tạp với sự chuyển dịch từ HP-PRRSV sang Lineage 1 (NADC30, NADC34). Bài viết này, Fivevet phân tích thực trạng và thách thức trong sử dụng vắc xin hiện nay.
 PRRSV có cấu trúc hệ gen như thế nào?
PRRSV có cấu trúc hệ gen như thế nào?IV. Vai trò của các dòng Lineage trong nghiên cứu và phát triển vắc xin
Mục tiêu quan trọng của nghiên cứu các gen và dòng di truyền của PRRSV là tạo ra vắc xin có khả năng bảo hộ chéo (cross-protection) rộng rãi. Tuy nhiên, thực tế cho thấy mức độ tương đồng về mặt di truyền (homology) không phải lúc nào cũng tỷ lệ thuận với mức độ bảo hộ thực địa.
4.1. Vắc xin sống nhược hóa (MLV) và thách thức về tính tương đồng
Vắc xin MLV hiện vẫn được sử dụng phổ biến nhờ khả năng tạo miễn dịch mạnh và kéo dài. Phần lớn các loại vắc xin MLV thương mại hiện nay được phát triển từ các chủng thuộc Lineage 5 (như VR-2332) hoặc Lineage 8 (như JXA1, HuN4).
Tuy nhiên, khi đối mặt với các chủng thực địa thuộc Lineage 1 mới nổi, hiệu quả của các loại vắc xin này thường bị suy giảm nghiêm trọng. Một nghiên cứu so sánh tại Việt Nam cho thấy, dù vắc xin dựa trên Lineage 8 có độ tương đồng di truyền cao hơn với chủng thách thức thực địa trong một số trường hợp, nhưng vắc xin dựa trên Lineage 1 hoặc Lineage 5 lại mang lại hiệu quả tăng trưởng và tỷ lệ sống tốt hơn cho lợn con. Điều này cho thấy sự bảo hộ phụ thuộc vào các epitope bảo tồn nằm rải rác trên nhiều protein khác nhau, chứ không chỉ riêng gene ORF5.
4.2. Phát triển vắc xin dựa trên Lineage 1 (NADC30-like và NADC34-like)
Trước sự càn quét của các chủng thuộc Lineage 1 tại Châu Á, các nhà khoa học đã tập trung phát triển các vắc xin trực tiếp từ dòng này. Chủng vắc xin nhược hóa SD-R, được phát triển từ một nhánh của Lineage 1.8, đã chứng minh khả năng bảo hộ chéo ấn tượng không chỉ chống lại các chủng NADC30-like và NADC34-like mà còn có hiệu quả đối với cả các chủng độc lực cao HP-PRRSV.
Sự thành công của SD-R mở ra một hướng đi mới: Thay vì cố gắng tạo ra một loại vắc xin cho mọi dòng, các nhà nghiên cứu đang tìm cách xác định các "dòng xương sống" có khả năng kích hoạt phản ứng miễn dịch rộng nhất. Thực tế cho thấy SD-R có thể làm giảm đáng kể tình trạng teo tuyến ức và tổn thương phổi do HP-like PRRSV gây ra là một minh chứng cho thấy sự bảo hộ chéo có thể đạt được nếu chọn đúng chủng đích.
4.3. Vắc xin Chimeric và công nghệ di truyền ngược
Công nghệ di truyền ngược cho phép các nhà khoa học “lắp ghép” gen từ nhiều dòng PRRSV khác nhau để tạo ra vi rút lai (chimeric), mang đặc tính kháng nguyên đa dạng, từ đó tăng khả năng bảo hộ.
- Chủng vắc xin lai JB1: Được tạo ra bằng cách thay thế các gen cấu trúc ORF3-6 của một khung xương ổn định bằng các đoạn gen tương ứng từ hai chủng PRRSV-2 khác biệt về mặt di truyền. Kết quả cho thấy lợn được tiêm phòng JB1 có khả năng bảo hộ đồng thời chống lại cả hai chủng bố mẹ, giúp cải thiện tỷ lệ sống và trọng lượng lợn con khi sinh.
- Tối ưu hóa khả năng thích ứng: Một trong những rào cản lớn khi phát triển vắc xin từ các dòng mới như NADC34-like là khả năng thích ứng kém của chúng trên các dòng tế bào nuôi cấy như MARC-145. Bằng cách thay thế vùng protein cấu trúc của chủng NADC34 thực địa bằng vùng tương ứng của một chủng vắc xin đã thích nghi tốt (như CH-1R), các nhà khoa học đã tạo ra chủng rNADC34-CHSps có khả năng nhân lên mạnh mẽ trong phòng thí nghiệm trong khi vẫn giữ được các epitope bảo vệ của chủng thực địa.
4.4. Cơ chế miễn dịch và các Epitope trung hòa
Hiệu quả của bất kỳ loại vắc xin nào cũng phụ thuộc vào khả năng kích hoạt các kháng thể trung hòa (NAs) và tế bào T nhớ nhắm vào các vị trí quan trọng trên vi rút.
Protein GP5: Mục tiêu chính và hiện tượng "lớp giáp Glycan"
GP5 là đích đến quan trọng nhất của các kháng thể trung hòa, nhưng vi rút đã phát triển những cơ chế phòng vệ tinh vi để vô hiệu hóa sự tấn công này. Trên vùng ectodomain của GP5, các nhà nghiên cứu đã xác định được:
- Epitope A (Mồi nhử): Đây là một epitope siêu biến đổi và chiếm ưu thế miễn dịch, nghĩa là cơ thể lợn sẽ ưu tiên sản sinh kháng thể chống lại vị trí này đầu tiên. Tuy nhiên, các kháng thể này không có tác dụng trung hòa vi rút, chúng đóng vai trò như một "lá chắn giả" để làm chệch hướng hệ miễn dịch của vật chủ.
- Epitope B (Trung hòa): Đây là vị trí bảo tồn hơn, nơi các kháng thể thực sự có khả năng tiêu diệt vi rút sẽ gắn vào. Đáng tiếc là epitope B thường bị bao phủ bởi các chuỗi đường (N-glycosylation), ngăn cản sự tiếp cận của kháng thể. Hiện tượng "glycan shielding" này giải thích tại sao lợn nhiễm PRRSV thường mất rất nhiều thời gian (ít nhất 3 tuần hoặc hơn) để bắt đầu xuất hiện kháng thể trung hòa.
Vai trò của các protein phụ trong việc xâm nhập tế bào
Các nghiên cứu gần đây đã làm thay đổi quan điểm tập trung duy nhất vào GP5. Phức hợp trimmer GP2-GP3-GP4 hiện được coi là thành phần quyết định việc gắn kết với thụ thể CD163 trên bề mặt đại thực bào. Do đó, các chiến lược vắc xin mới đang cố gắng bao gồm cả các protein này để tạo ra một hàng rào miễn dịch đa lớp, ngăn chặn vi rút ngay từ giai đoạn bám dính vào tế bào.
V. Tình hình dịch tễ và thực tiễn sử dụng vắc xin tại Việt Nam
Việt Nam là một trong những quốc gia chịu ảnh hưởng nặng nề bởi PRRSV tại Đông Nam Á, với sự thay đổi liên tục của các dòng vi rút theo thời gian, gây khó khăn lớn cho công tác phòng chống.
5.1. Sự chuyển dịch từ HP-PRRSV sang Lineage 1
Từ năm 2007, các chủng HP-PRRSV (Lineage 8.7) đã gây ra các đợt dịch tàn khốc với tỷ lệ chết cực cao. Tuy nhiên, trong những năm gần đây, các chủng thuộc Lineage 1 (NADC30-like và gần đây là NADC34-like) đã bắt đầu xuất hiện và lan rộng. Dữ liệu giám sát cho thấy sự tồn tại song song của nhiều dòng di truyền trong cùng một khu vực địa lý, thậm chí trên cùng một cá thể lợn.
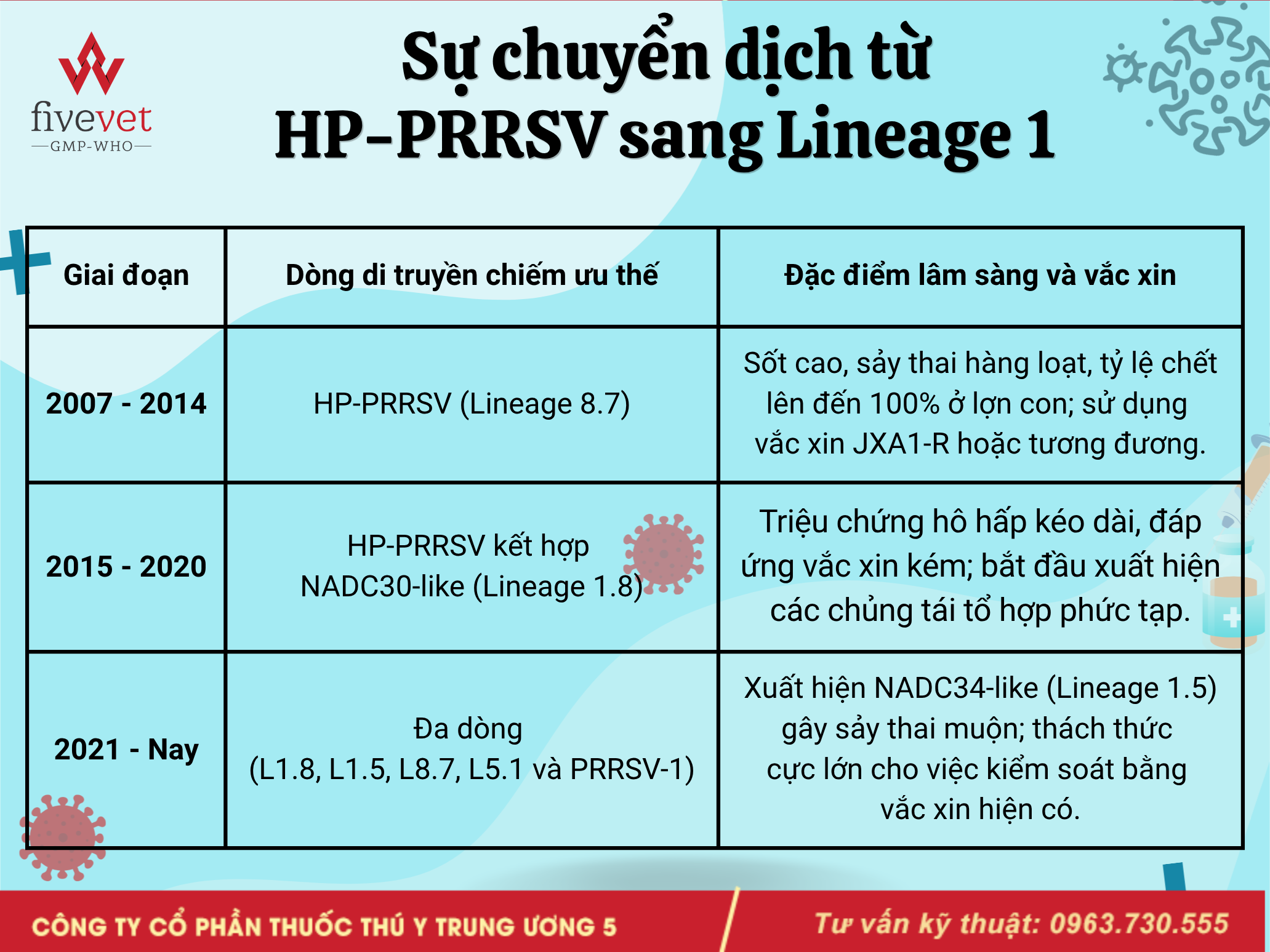
Sự chuyển dịch từ HP-PRRSV sang Lineage 1
5.2. Thách thức đối với các hộ chăn nuôi nhỏ lẻ
Tại Việt Nam, chăn nuôi quy mô nhỏ chiếm khoảng 70% tổng sản lượng, nhưng lại là nhóm ít sử dụng vắc xin PRRS do hạn chế về kinh tế và nhận thức an toàn sinh học.
Việc không tiêm phòng đầy đủ hoặc sử dụng vắc xin không phù hợp không chỉ gây thiệt hại trực tiếp cho người chăn nuôi, mà còn biến các hộ nhỏ lẻ thành nguồn lưu trữ vi rút. Đây là điều kiện để PRRSV tiếp tục đột biến, tái tổ hợp và sau đó lây lan sang các trang trại lớn, làm gia tăng nguy cơ bùng phát dịch trên diện rộng.
VI. Các công nghệ vắc xin tiên tiến và tầm nhìn tương lai
Trước hiệu quả hạn chế của vắc xin truyền thống đối với các chủng Lineage 1 mới nổi, ngành thú y đang hướng đến các công nghệ vắc xin hiện đại, giải pháp đột phá hơn.
6.1. Vắc xin mRNA và DNA
Công nghệ mRNA, vốn đã chứng minh hiệu quả rực rỡ trong đại dịch COVID-19, đang được ứng dụng để phát triển vắc xin PRRSV. Ưu điểm của mRNA là khả năng sản xuất nhanh chóng, an toàn (không chứa vi rút sống) và có thể dễ dàng thay đổi trình tự để phù hợp với các biến thể mới nổi trong thời gian thực. Vắc xin DNA cũng là một hướng đi tiềm năng, tập trung vào việc kích hoạt miễn dịch tế bào mạnh mẽ thông qua việc biểu hiện các protein vi rút trực tiếp trong tế bào lợn.
6.2. Công nghệ PROTAC và vắc xin nhược hóa thế hệ mới
Công nghệ Proteolysis-targeting chimeras (PROTAC) cung cấp một phương pháp hoàn toàn mới để làm nhược hóa vi rut. Bằng cách chèn các đoạn mã (PTD - Proteasome-targeting domain) vào hệ gen vi rút, các protein của vi rút sau khi được tổng hợp sẽ bị proteasome của tế bào vật chủ nhận diện và phân hủy ngay lập tức. Điều này cho phép vi rút vẫn có thể xâm nhập và kích hoạt hệ miễn dịch nhưng không thể nhân lên đủ mạnh để gây bệnh, đồng thời tạo ra một lượng lớn các peptide kháng nguyên để trình diện cho tế bào T CD8+, dẫn đến phản ứng miễn dịch cực kỳ mạnh mẽ.
6.3. Vắc xin đa giá và tá dược (Adjuvants) hiện đại
Xu hướng phát triển vắc xin đa giá (multivalent), kết hợp kháng nguyên từ nhiều dòng (ví dụ: Lineage 1, Lineage 8 và PRRSV-1) đang được coi là chiến lược thực tế nhất để đối phó với tình trạng đa dòng thực địa. Bên cạnh đó, việc phát triển các tá dược mới có khả năng kích thích các thụ thể nhận diện mẫu (PRRs) giúp tăng cường tính miễn dịch cho các loại vắc xin subunit hoặc vắc xin chết (KV) vốn có hiệu quả thấp trước đây.
VII. Định hướng kiểm soát PRRSV trong chăn nuôi hiện đại
PRRSV là minh chứng điển hình cho khả năng thích nghi và tiến hóa nhanh của vi rút ARN. Việc hiểu rõ hệ gen và các dòng lineage không chỉ mang ý nghĩa nghiên cứu mà còn là cơ sở quan trọng giúp bác sĩ thú y và người chăn nuôi đưa ra quyết định phòng bệnh hiệu quả.
Dựa trên các phân tích khoa học, các chiến lược kiểm soát PRRSV trong tương lai cần tập trung vào:
- Giám sát di truyền dựa trên Lineage: Việc chỉ xét nghiệm PCR "dương tính" hay "âm tính" là không đủ. Các trang trại cần thực hiện giải trình tự gene ORF5 thường xuyên để biết chính xác chủng vi rút đang lưu hành thuộc dòng nào, từ đó lựa chọn loại vắc xin phù hợp nhất.
- Thận trọng với việc sử dụng đồng thời nhiều loại MLV: Để tránh rủi ro tái tổ hợp tạo ra các chủng vi rút vắc xin mới nguy hiểm, cần có khoảng cách thời gian hợp lý và quy trình quản lý chặt chẽ khi thay đổi hoặc sử dụng kết hợp các loại vắc xin sống.
- Ưu tiên các vắc xin có bảo hộ chéo rộng: Sự xuất hiện của các chủng như SD-R cho thấy khả năng bảo hộ chéo giữa các dòng khác nhau là có thể đạt được. Cần đẩy mạnh việc thương mại hóa các chủng vắc xin này để đối phó với tình hình dịch tễ phức tạp tại Châu Á.
- Kết hợp với an toàn sinh học: Vắc xin không thể thay thế hoàn toàn các biện pháp phòng dịch. Trong bối cảnh vi rút liên tục tái tổ hợp và thoát miễn dịch, các biện pháp an toàn sinh học nghiêm ngặt vẫn là hàng rào bảo vệ quan trọng nhất để ngăn chặn sự xâm nhập của các dòng vi rút lạ vào đàn lợn.
Kiểm soát PRRSV là một quá trình lâu dài, Chỉ khi kết hợp hiểu biết về di truyền của vi rút và ứng dụng linh hoạt các công nghệ vắc xin mới dựa trên phân loại lineage, ngành chăn nuôi mới có thể hy vọng kiểm soát và tiến tới loại trừ loại vi rút nguy hiểm này.
Bài viết được biên soạn bởi Phòng Nghiên cứu phát triển Vắc xin - Công ty cổ phần thuốc thú y Trung ương 5 (Fivevet).
Câu hỏi thường gặp:
1. Tình hình dịch PRRS tại Việt Nam hiện nay như thế nào?
PRRS tại Việt Nam đang diễn biến phức tạp với sự lưu hành đồng thời nhiều dòng vi rút, đặc biệt là sự gia tăng của Lineage 1 (NADC30-like, NADC34-like).
2. Vì sao Lineage 1 (NADC30, NADC34) lại đáng lo ngại?
Các chủng này có khả năng tái tổ hợp cao, gây triệu chứng phức tạp và làm giảm hiệu quả của các loại vắc xin truyền thống.
3. Những thách thức lớn nhất khi sử dụng vắc xin PRRS hiện nay là gì?
Bao gồm: vi rút biến đổi nhanh, không phù hợp chủng vắc xin, nguy cơ tái tổ hợp và điều kiện chăn nuôi chưa đảm bảo.
4. Vì sao cần giám sát lineage PRRSV tại trại nuôi?